

| Detecting HPV |
| HPV DNA testing in clinical practice |
| Immune response |
| Clinical trials and vaccines |
A human papillomavírusok és a méhnyakrák összefüggése
A Human Papilloma Vírusok a papovavírusok családjának tagjai. Jellemzõjük , hogy a laphám Malpighi-rétegében sejtproliferációt okozhatnak, a legtöbb vírusrészecskét az elszarusodó sejtek tartalmazzák, ennek eredményeként jóindulatú papillomatosus elváltozások alakulhatnak ki a genitáliákon, a felsõ légutakban, a tápcsatornában és a bõrön. Több, mint 70 különbözõ HPV típust azonosítottak DNS molecularis hybridizációval különbözõ régiókból származó szemölcsös léziókból. A vírusok erõs szövetspecificitást mutatnak, mely genetikailag meghatározott. Az anogenitalis szemölcsök és a cervicalis biopsziákból történt molecularis genetikai vizsgálatokkal a 70 vírus típusból körülbelül 30-at azonosítottak a nõi nemiszerveken.
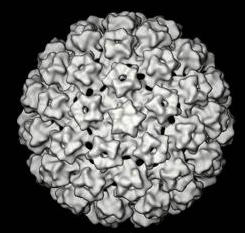 |
| A Human Papillomavirus elektronmikroszkópos képe. |
A papillomavírusok 45-55 nm átmérõjũ, kubikalis szimmetriájú, burok nélküli, gömb alakú virionok, amelyeknek kettõs fonalú körkörös DNS-ét 72 kapszomer borítja. A DNS-ben három funkcionális régió kódolt: E- a korai vírus fertõzés funkció, L- késõi vírus fertõzés funkció, LCR- a két szakasz közti régió.
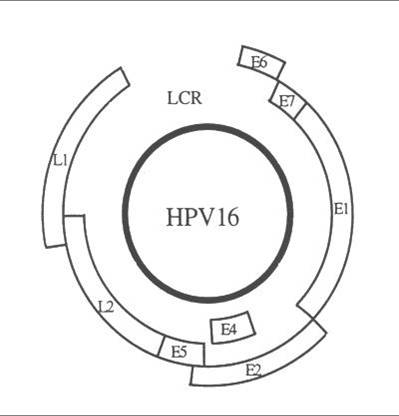 |
| HPV 16 genom strukturája: a kódoló regiokat nyitott keretekkel jeleztük (Phillips AC and Vousden KH 1998) |
| Gene/Region | Function |
E1/E2 |
Az E6 E7 genek mũködését ellenõrzõ fehérjét meghatározó gén |
| E4 | Funkciója alig ismert, valószinũleg a virus sejtbõl történõ kiszabadulásában van szerepe. |
| E5 | Olyan hydrophob proteint kódol, ami a sejt immortalizációját fokozza. |
| E6 | Olyan proteineket kódol, amelyek a sejtciklus negatív szabályozását gátolják. Az E6 gén terméke a P53 mũködését gátolja.Ez utóbbi az apoptozis transkripciós faktora (a programmozott sejthalál folyamatát gátolja) |
| E7 | Az ezálltal kódolt termék a retinoblastoma tumor supressor fehérjékez kötõdik. Ez teszi lehetõvé, hogy a sejt normál mitogén jelek hiánya mellett is folyamatosan szaporodjon. |
| L1/L2 | Strukturális fehérjét kódol ami felelõs a virus tokjának összeállításáéert. |
| LCR | A normális virus replikációhoz és a gén expressió kontrolljához szükéges |
A cervix hám HPV fertõzésének szövettana, a fertõzéssel járó morfológiai elváltozások
HPV fertõzés keletkezésének jellemzõ életkora: HPV az egyik leggyakoribb nemi úton terjedõ betegség. 50 éves korukra a nõk 75%-a legalább egy HPV fertõzésen már átesett. Legmagasabb a fertõzöttség a kora tizenévesekben és a huszonévesekben. Ezt követõen a gyakoriság csökken, valószinũleg a virussal szembeni immunitás hatására. Mindemellett a virus fennmaradhat mint latens infekció kicsiny góca, ilyenkor csak molekuláris szinten detektálható..
Fertõzés útja: a HPV a hám basalsejtes rétegén keresztül hatol be (általában az átmeneti zónában) és itt a bazalis sejtek osztódásával párhuzamosan a virus replikálódik. A virus perzisztálhat a bazalis sejtrétegben latens (inaktiv) formában, vagy a sejtéréssel párhuzamosan folytathatja szaporodását. A hámrétegben annak érésével párhuzamosan felismerhetõvé válik a virus citopátiás hatása mind a szövettani mind a citológiai készitményekben: koilocitozis, parakeratozis és egyes sejt keratinizációja formájában. Az akut fertõzés spontán regrediálhat a léziók gyógyulásával de mint lateens infekció perzisztálhat is. Az ilyen fertõzés késõbb bármikor rektiválódhat.
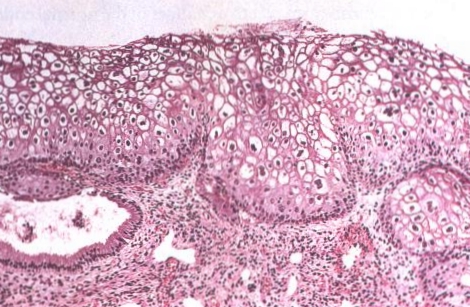 |
| LSIL (CIN1) : lapos condylomaként is ismert, koilocitás atypia jellemzi. általában HPV6 HPV11 fertõzés kapcsán alakul ki. |
Bizonyitékok, melyek azt támsztják alá, hogy a HPV fertõzésnek szerepe van a carcinogenezisben.
1977-ben elsõként vetette fel két közlemény, hogy humán papilloma virusok a cervix epitheliumban jelen lehetnek (Meisels & Fortin 1977; Purola & Savia 1977) Ugyanezek szerzõk hivták fel a figyelmet koilociták jelenlétére CIN léziókat is mutató cervix kenetekben ill, biopsziákban. Az elváltozásokat "lapos kondyloma " lapos szemölcs vagy kondilomás szemölcs névvel illették.További tanulmányok megerõsítették virus antigen és HPV DNS jelenlétét fokális CIN1 lézióhóz kapcsoltan.Ezek a megfigyelések inditották el azokat a munkákat, amelyek a HPV daganat keletkezésében betöltött szerepével foglalkoztak ((Coleman and Richman 1983).
Az anogenitális szemölcsök, a CIN ill. malignus méhnyak szövet vizsgálata alapján a virusok két csoportba oszthatók: az egyik csoportba tarozók low grade CIN leziók és exophitikusan növekvõ anogenitális folyamatokat jellemeznek, ; ezek malignus tumorrá alakulása igen alacsony kockázatú. A virusok másik csoportját a CIN 2, CIN3 és CIS elváltozásokban lelték. Ezért nevezzük ezen virusokat a daganatos átalakulásban és az azt megelõzõ állapotokban elõforduló magas rizikóju viruscsaládnak.
Az eltérõ virus csoportok daganat keltõ képességét kiterjedten tanulmányozták, az alábbiakban még jelen anyag is tárgyalja.
HPV tipusok, melyeket a nõi nemi szervekben találtak.
| High risk | |
| 16,18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68 may lead to Invasive Cancer | |
| Low risk | |
| 6, 11, 42, 44, 53, 54, 62, 66 may lead to condylomata | |
HPV onkogén képessége
A virus génjeinek a hámsejtek tulajdonságait befolyásoló képességét sokat tanulmányozták, igy kiderült, hogy a high risk virusok figyelemre méltó onkogén képességgel bírnak. In vitro kísérletekben, human laphámsejteket (amelyek a HPV virus természetes célpontjai) alacsony és magas rizikójú (low risk, high risk) HPV tipusokkal fertõztek. A magas kockázatú HPV16 és HPV 18 virusfertõzést követõen ezen virusok a humán laphámsejteket immortalizálták, azaz élettartamukat meghosszabbították ("halhatatlan" sejtek") HPV 16 virus hatására ez nem következett be: ezen laphámsejtek élettartama nem változott, szabályos érési folyamatot követõen elpusztultak. Rágcsálók sejtjeiben hasonló események zajlanak fertõzés hatására. U.n. raft tenyészetekben, ("organotyp", speciális tenyésztõ oldat alkalmazásakor) a HPV18 által fertõzött sejtek a CIN lezióhoz hasonló elváltozásokat mutatnak.
A legmeggyõzõbb bizonyíték arra, hogy a HPV virusok kulcs szerepet játszanak a daganat keletkezésében azon alapszik ahogyan a HPV DNS képes a cervikális sejtekbe integrálódni. Amig a HPV DNS condyloma és LG CIN esetében általában episomalisan helyezkedik el (a sejtmagtól függetlenül), rák sejtjeiben a virus DNS integrálódik a gazdasejt genetikai állományába (genomjába).Az integráció következtében az E1 és E2 gének expressioja károsodik, ezek a gének kontrollálják normális körülmények között az E6 E7 géneket. Az E1/ E2 gén károsodás következtében az E6 és E7 gének deregulációja következik be. Az E6 és E7 gének kódoló regioja felelõs a P53 és Rb daganat supressor gének hibátlan mũködéséért. Amennyiben ez a fentiek értelmében károsodik a sejtek kikerülnek a normál sejtciklus szabályozó rendszerének ellenõrzése alól a ciklus G1 és G2 fázisában, ami kontrollálatlan sejt növekedéshez vezet
A DNS integrációja mindíg fellelhetõ jelenség HPV 16 és HPV 18 virust tartalmazó rákokban. Ez bizonyítjaq leginkább, hogy a HPV16 és HPV 18 a cervix rák keletkezésében kulcs szerepet játszik. HPC DNS az invaziv méhnyakrákok 90%-ában jelen van.
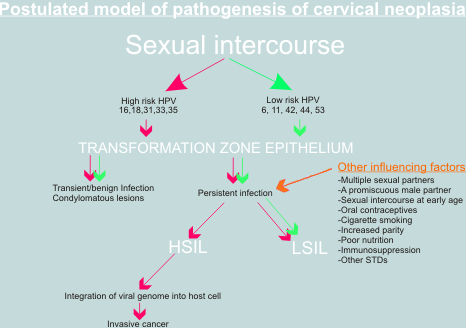 |
Járulékos (Ko-) faktorok fontossága
Széles körben elfogadott álláspont, hogy önmagában a HPV fertõzés de még csupán a DNS integrációja önmagában sem elegendõ ahhoz, hogy a sejt daganatsejtté alakuljon. Genitális HPV16 fertõzés gyakori, a cervix rák ugyanakkor ritka; HPV integrációt lapos szemölcsök és egyszerũ CIN léziók esetében többször megfigyeltek ugyanakkor. A feltételezett kisérõ hatások (ko faktorok): gátolt immun védekezés, a virus perzisztálása a sejtben, dohányzás, szteroid hormon hatás (fogamzásgátló tabletta) lehetnek. A ras és fos és egyéb onkogének mutációját is észlelték cervix rákban, de in vivo szerepük még bizonyításra szorul. Jelen tudásunk hiányosságai ellenére bizonyos, hogy a papilloma virusok tanulmányozása mindededig egyedülálló betekintést adott a tudomány számára a cervix rák keletkezésének folyamatába. Mindezen tudás hasznos a jövõben mind a prevenció (vaccináció), mind a korai diagnozis (HPV DNS szũrés) és a kezelés megismerése (antivirális szerek) szempontjából.
HPV fertõzés a cervix rák összefüggése: relative kockázat igen erõs, összehasonlítható a chronikus B hepatitis és májrák összefüggésében észlelt kockázattal, de mindenképpen kifejezettebb mint a dohányzás és tüdõrák esetében.