| Wykrywanie HPV |
| Test HPV DNA w praktyce klinicznej |
| Odpowiedź Immunologiczna |
| Testy kliniczne i szczepionki |
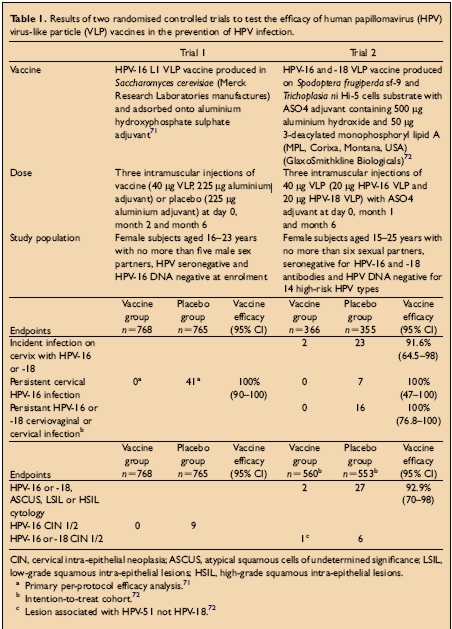
Badania kliniczne nad zastosowaniem szczepionki przeciw wirusowi HPV.
Przeprowadzono dwa duże randomizowane badania kliniczne metodą podwójnie ślepej próby nad zastosowaniem szczepionki przeciw HPV. W obydwu badaniach po szczepieniu HPV VLPs stwierdzono odpornośc na przetrwałą infekcję HPV i na wystąpienie zmian chorobowych szyjki macicy wywołanych przez homologiczne wirusy HPV.
Williamson et al
Stratergies for the prevention of cervical cancer by human papillomavirus vaccination
Best Practice & Research Clinical Obstetrics & Gynaecology (2005) 19-4 pp531-544
Badanie 1: Przetrwala infekcje HPV zdefiniowano jako obecnosc DNA HPV16 w 2 lub 3 próbkachBadanie 2: Przetrwala infekcje HPV 16/18 zdefiniowano jako obecnosc takiego samego genotypu wirusa wyizolowanego metoda PCR przynajmniej dwukrotnie na przestrzeni 6 miesiecy
For further information about the conduct of the trials consult:
LA Koutsky,KA Ault and CM Wheeler et al
A controlled trial of a human papillomavirus type 16 vaccine
New England Medical J (2002) 347 (pp1757-1765DM Harper,EL Franco and C Wheeler et al
Efficacy of a bivalent L1 virus-like particle vaccine in prevention of infection with HPVtypes 16 and 18 in young women: a randomised controlled trial.
Lancet (2004) 364pp1757-1765Nowa szczepionka przeciw HPV
Gardasil jest pierwszą szczepionką przeciw rakowi szyjki macicy wyprodukowaną w Europie przez firmę Sanofi Pasteur/ Merck and Co. Szczepionka ma chronic przed zakażeniem HPV 6, 11, 16 i 18, które są najczęstszą przyczyną występowania kłykcin i raka szyjki macicy. W dużym badaniu klinicznym przeprowadzonym u kobiet w wieku 16 - 23 lata bez cech zakażenia HPV przed badaniem, nie stwierdzono zakażenia tymi wirusami ani raka szyjki macicy po okresie 5 lat od zakończenia badania.Szczepionka została zatwierdzona do użytku klinicznego przez Amerykańską Agencję żywności i Leków (Food and Drug Agency, FDA) w czerwcu 2006. Kilka miesięcy pózniej Europejska Agencja Medyczna (European Medical Agency, EMEA) wydała licencję pozwalającą na stosowanie szczepionki w 25 krajach Unii Europejskiej. Do innych krajów, w których zatwierdzono stosowanie Gardasilu należą Kanada, Meksyk, Brazylia, Australia i Nowa Zelandia.
W związku z tym, że zakażenie HPV należy do częstych chorób przenoszonych drogą płciową, szczepionka powinna być stosowana u dziewcząt, które jeszcze nie rozpoczęły życia płciowego. Działanie szczepionki jest maksymalnie efektywne u dziewcząt i młodych kobiet szczepionych przez ekspozycją na HPV. Taki sposób postępowania został zaakceptowany przez FDA, EMEA i agencje narodowe. Amerykański Komitet Doradczy ds. Szczepień (American Advisory Committee on Immunisation Practices, ACIP) poszedł jeszcze dalej proponując, aby Gardasil został umieszczony w kalendarzu szczepień dziewczynek w wieku 11-12 lat.
Reakcja służby zdrowia, polityków, feministek i innych zainteresowanych organizacji na wiadomośc o nowej szczepionce była różna. W listopadzie 2006 roku rząd Australii ogłosił bezpłatne szczepienia w 2007 roku dla wszystkich dziewczynek i kobiet od 12 do 26 roku. Podobne działania przeprowadził rząd Niemiec. W USA, w 20 stanach uregulowano prawnie koniecznośc wykonania obowiązkowych szczepień u dziewcząt w wieku 10 - 12 lat. Napotkało to sprzeciw ze strony opozycji, czyli pracowników służby zdrowia, polityków, feministek, którzy twierdzili, że jest to naruszenie praw rodzicielskich. Inni twierdzili, że stosowanie u nastolatek szczepionki przeciw chorobie przenoszonej drogą płciową będzie promowało swobodę seksualną.Ginekolodzy i pracownicy służby zdrowia wyrażają obawy co do staosowania szczepionki. Szczepionka nie była badana w kierunku odległych działań ubocznych ani czasu utrzymywania się odporności na zakażenie HPV 6, 11, 16, 18. Niezbędne jest prowadzenie dalszych długoterminowych badań aby ocenic, czy sama szczepionka zapobiega rozwojowi raka szyjki macicy. Firma Merck and Co, która wyprodukowała szczepionkę zaznacza, że szczepionka zapobiega tylko 70% rakom szyjki macicy. Produkcja szczepionki, która całkowicie zapobiegłaby rakowi szyjki macicy będzie dużym wyzwaniem dla producentów.
Firma Merck and Co wyjaśnia, że kobiety, które otrzymały szczepionkę powinny dalej wykonywac badania cytologiczne w ramach skryningu raka szyjki macicy. Istnieje niebezpieczeństwo, że szczepionka da kobietom fałszywe poczucie bezpieczeństwa co obniży zgłaszalnośc na badania cytologiczne. Z zastrzeżeń przedstawionych powyżej wynika także potrzeba rejestracji i ciągłego monitorowania wszystkich kobiet, które były szczepione.