(liquid based cytology, LBC)
| Wprowadzenie |
| Wymagania |
| Podstawowe elementy systemu skanowania |
| Rodzaje instrumentów |
| Cytologia fazy plynnej (LBC) |
Cytologia fazy płynnej.
Zasady przygotowania preparatów w technologii cytologii fazy płynnej (LBC)
- Materiał jest pobierany z szyjki macicy przy pomocy szpatułki lub szczoteczki.
- Pobrany materiał jest umieszczony w pojemniku zawierającym płyn - utrwalacz/medium do transportu.
- Komórki są zawieszone w płynie
- Preparaty są sporządzane z osadu płynu
- Komórki są osadzane na szkiełku mikroskopowym przez cytowirowanie, metodą filtracji lub sedymentacji, gdzie tworzą jedną warstwę komórek.
- Rozmazy są barwione i nakrywane szkiełkami nakrywkowymi
Obecnie dostępnych jest kilka systemów LBC. Najbardziej szeroko stosowane to:
- Sure Path (autocyte, TriPath Imaging)
- Thin Prep (CYTYC)
Charakterystyka systemów Surepath i Thinprep
Tradycyjne rozmazy cytologiczne versus LBC - różnice w pobieraniu materiału przygotowaniu rozmazów
Conventional preparation Liquid based preparation Zalety LBC
Wady LBC
Adekwatność preparatów LBC
Wszystkie badania przeprowadzone w Wielkiej Brytanii wykazały, że odsetek preparatów nie nadających się do oceny cytologicznej jest niższy w przypadku preparatów LBC. Podobnie w innych krajach wykazano, że odsetek ten jest zmienny. Wyniki tych badań miały istotne znaczenie w podjęciu decyzji o wprowadzeniu preparatów LBC w miejsce tradycyjnych preparatów cytologicznych. Zaniepokojenie budził jednak fakt, niskiego odsetka rozmazów nie nadających się do oceny. Czy ten niski odsetek wynika z przeklasyfikowania rozmazów nie nadających się do oceny w metodzie tradycyjnej na ujemne i nadające się do oceny w metodzie LBC? Czy niski odsetek rozmazów nie nadających się do oceny nie powoduje obniżenia odsetka rozmazów zawierających komórki nieprawidłowe? Pytania pozostają na razie bez odpowiedzi. Konieczne jest prowadzenie dalszych badan celem ustalenia kryteriów dla rozmazu odpowiedniego do oceny w metodzie LBC. Aktualne stosowane kryteria oceny adekwatności rozmazu są subiektywne i różnią się znacznie pomiędzy pracowniami, co powoduje ich słabą standaryzację.
Kryteria Bethesda do oceny adekwatności preparatów LBC.
- Każdy preparat zawierający komórki nieprawidłowe jest z definicji rozmazem nadającym się do oceny
- W rozmazie musi znajdować się co najmniej 5000 dobrze zachowanych komórek nabłonka wielowarstwowego płaskiego
- Ocenionych powinno być co najmniej 10 pół widzenia przy zastosowaniu obiektywu 40x. Należy oceniać pola widzenia poruszając się wzdłuż średnicy obszaru zajętego przez komórki łącznie z oceną środka preparatu.
- Preparaty, w których stwierdza się mniej niż 5000 komórek powinny być ocenione celem wskazania przyczyny małej liczby komórek
- Tabela przestawia średnią liczbę komórek w polu widzenia odpowiadającą 5000 komórek w preparacie LBC. Jeżeli w preparacie stwierdza się obszary ubogokomórkowe albo pozbawione komórek, przy ustaleniu rozpoznania należy uwzględnić odsetek obszarów ubogokomórkowych.
Zobacz szybką metodę oceny komórkowośći rozmazu 1
Zobacz szybką metodę oceny komórkowośći rozmazu 2
Zmiany morfologii komórek w preparatach LBCGłówne zmiany w morfologii komórek nabłonkowych w preparatch LBC to:
- utrata połączeń międzykomórkowych i przypadkowe rozproszenie komórek
- rozproszenie komórek nieprawidłowych
- nieliczne komórki ułożone w jednej warstwie mogą być trudne do skryningu i interpretacji
Zmiany te przedstawiono na zdjęciach poniżej.
Ogólny obraz rozmazu
Rozkład komórek w rozmazie jest wyeliminowany - ale budowa komórki i należące do kontekstu tło są podobne do konwencjonalnego rozmazu. Tło jest bardziej czyste niż w rozmazie konwencjonalnym, co ułatwia identyfikacje komórek prawidłowych i nieprawidłowych. Krew, śluz, wysięk zapalny i martwicze resztki komórek można także rozpoznać w preparacie LBC, mimo że wyglądają trochę inaczej i niż w rozmazie konwencjonalnym .
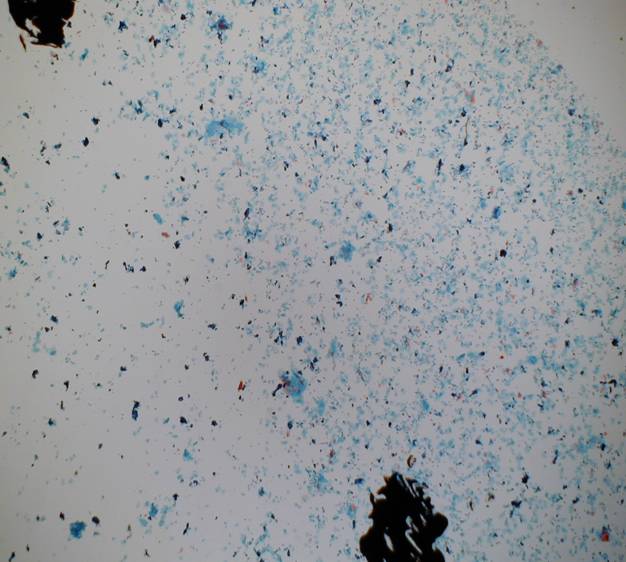
Nieodpowiedni LBC
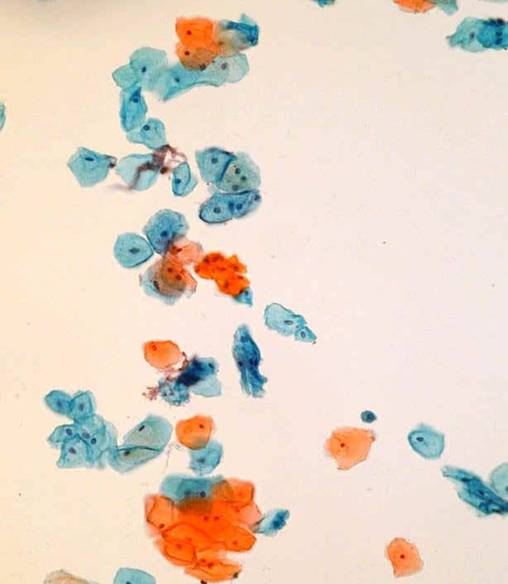
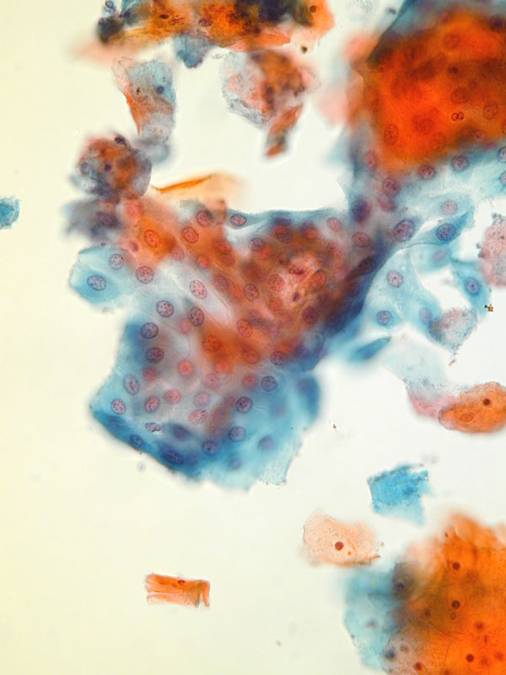
Odpowiedni LBC Komórki nabłonka wielowarstwowego płaskiego
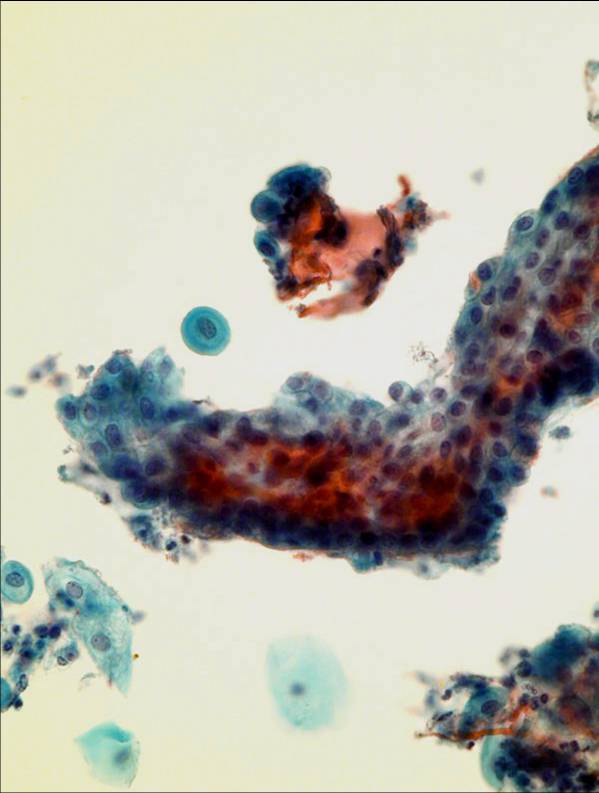
Ogólnie morfologia komórek nowotworowych jest zachowana, chociaż występują one głównie w postaci izolowanych komórek. Gniazda i płaty komórek są generalnie mniejsze niż te, które widuje się w preparatach konwencjonalnych. Komórki kanału szyjki i niedojrzałej metaplazji wydają się nieco mniejsze. Chromatyna wydaje sie byc bardziej ziarnista, ale równomiernie rozłożona. Błona jądrowa jest zazwyczaj cienka, ale może być pofałdowana. Komórki endocerwikalne
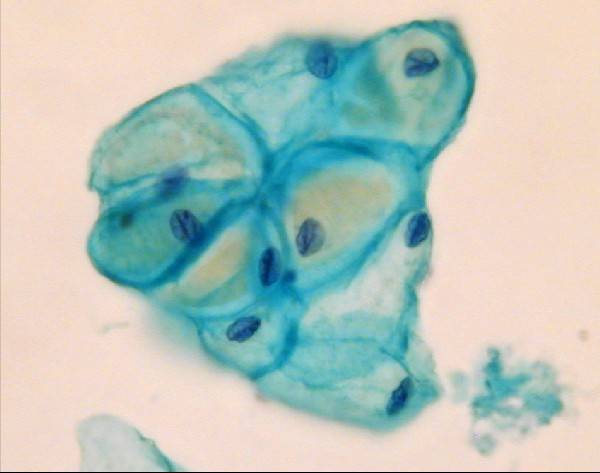
Typowe struktury plastra miodu mogą być widywane, chociaż znajduje się także komórki izolowane i w postaci układów palisadowych. Nagie jądra występują rzadziej w preparatach LBC. Jądra wydają się obkurczone i chromatyna bardziej ziarnista. Rzęski i wakuole śluzowe w cytoplazmie są również widoczne. Niekiedy komórki mogą być bardziej zaokrąglone lub skręcone, co stanowi artefakt procesu technologicznego. Niedojrzałe komórki metaplastyczne
Komórki endometrialne zwykle są dobrze zachowane w preparatach LBC w porównaniu z tradycyjnymi preparatami cytologicznymi, gdzie wydają się wykazywać cechy zwyrodnienia. Występują one w trójwymiarowych zlepach, w postaci kul ale mogą także występować pojedynczo. Jądra komórkowe są owalne lub okrągłe, małe, równe i hiperchromatyczne. W preparatach LBC pobranych w czasie miesiączki stwierdza się lizę erytrocytów, co manifestuje się obecnością wyługowanych erytrocytów. Mogą być także widoczne histiocyty i debris komórkowe.
- Krew ulega lizie, dlatego w preparatach LBC pobranych w czasie miesiączki stwierdza sie wyługowane erytrocyty
- Komórki występują w przezroczystych, trójwymiarowych zlepach
- Lepiej widoczna jest ziarnista struktura chromatyny i nieregularny obrys błony jądrowej
Ciąża
Ocena preparatów LBC w Anglii - badanie pilotażowe
- W czerwcu 2000 roku National Institute for Clinical Excellence (NICE) opublikował wytyczne dotyczące stosowania preparatów LBC w skryningu cytologicznym
- Wykazano, że ze stosowania preparatów LBC płynie znaczna korzyść, ale wyniki badań są różne i ciągle pewne zagadnienia są niewyjaśnione
- Zaproponowano program pilotażowy wprowadzenia preparatów LBC z dokładną oceną każdego z etapów tego programu.
- Celem projektu miała być ocena wyników, kosztów i skutków zastosowania preparatów LBC w skryningu cytologicznym
- Producenci dwóch systemów ThinPrep® i SurePath aplikowali o stosowanie ich systemów w badanich pilotażowych. W dwóch ośrodkach został zastosowany system ThinPrep® a w jednym SurePathT.
- W ramach badań pilotażowych przeprowadzonych w latach 2001-2002 oceniono 250 000 preparatów (i wykonano około 12 500 testów HPV). Wyniki tych badan były porównywalne z wynikami tradycyjnych badań cytologicznych przeprowadzonych w okresie poprzedzającym.
- Ponadto przeanalizowano koszty związane z zakupem nowego sprzętu, innych materiałów, pracy ludzkiej, testów HPV oraz oceniono reakcje psychologiczne u kobiet z rozmazem, nie nadającym się do oceny ale z dodatnim wynikiem testu na obecność HPV.
Wyniki badania pilotażowego nad wprowadzeniem preparatów LBC w Anglii - cd.
- Wprowadzenie preparatów LBC spowodowało spadek odsetka rozmazów nie nadających się do oceny cytologicznej z 9% na 1-2%. Odsetek rozmazów nie nadających się do oceny był niższy przy stosowaniu SurePathT niż przy stosowaniu ThinPrepT.
- Nie ma przekonywujących dowodów co do związku między preparatami LBC a odsetkiem rozmazów granicznych, rozmazów z cechami śródnabłonkowej neoplazji małego, średniego i dużego stopnia
- Stwierdzono wyższy odsetek zmian granicznych oraz rozmazów z cechami śródnabłonkowej neoplazji małego i średniego stopnia w ciągu dwóch pierwszych miesięcy trwania badania (efekt: "learning curve").
- Stwierdzono obniżenie odsetka rozmazów, w których rozpoznawano komórki nowotworowe pochodzenia gruczołowego.
- Nie można ocenić czułości badania pilotażowego, ponieważ nie były dostępne dane odnośnie liczby rozmazów fałszywie ujemnych ale analiza odsetków rozmazów z rozpoznaniem CIN1 i CIN2 oraz wstępna ocena dodatniej wartości predykcyjnej sugeruje, że czułość metody LBC nie jest mniejsza niż tradycyjnej cytologii szyjki macicy.
- Stwierdzono wzrost wydajności w pracowniach cytologicznych - więcej preparatów mogło być ocenionych w ciągu godziny.
- Obniżenie odsetka rozmazów LBC nie nadających się do oceny zredukuje koszty skryningu, ponieważ zmniejszy się liczba rozmazów, które trzeba ponownie pobrać, zabarwic i ocenić. Przykładowo zmniejszenie odsetka rozmazów nie nadających się do oceny z 9% do 1,6% w pracowni, w której do tej pory oceniano 30 000 rozmazów rocznie spowoduje zmniejszenie o 2200 liczby rocznie ocenianych rozmazów. W skali całego kraju doprowadzi to do zmniejszenia liczby ocenianych rozmazów z 4,2 mln do 3,9 mln.
Ocena preparatów LBC w innych krajach
- Narodowe programy skryningu cytologicznego są złożone i wielodyscyplinarne. W poszczególnych krajach skryningowe badania cytologiczne wykonywane są w różnych odstępach czasowych, dlatego ocena skutków wprowadzenia metodyki LBC będzie różna. Z oceny preparatów LBC przeprowadzonych w Australii, Nowej Zelandii, Niemiec, Francji, Holandii i Szkocji płyną różne wnioski.
- Szkocja wprowadziła metodykę LBC
- Australia i Nowa Zelandia zadecydowały, aby nie finansować badań wykonywanych metodą LBC z funduszy publicznych
- Niemieckie Towarzystwo Cytologii zaleca dalsze badania, a Francja nie opublikowała jeszcze żadnego raportu.
- W związku z tym, że obrazy cytologiczne w preparatach LBC różnią się od tradycyjnych obrazów cytologicznych, dlatego istotnym staje się przeprowadzenie szkoleń w zakresie interpretacji tych rozmazów
- Obecnie firmy produkujące zestawy do przygotowywania preparatów LBC oferują 3 dniowe szkolenie, których celem jest szkolenie instruktorów.
- Cytotechnicy biorący udział w szkoleniu po powrocie do swoich pracowni będą szkolić pozostałych cytotechników.
- Celem szkolenia cytotechników jest osiągnięcie czułości wykrywania HSIL na poziomie 95%, przed podjęciem skryningu metodą LBC
Zmiany w dotychczasowych procedurach (ciąg dalszy oceny preparatów LBC w Anglii)
- Przygotowanie preparatów LBC odbywa się automatycznie, sporządzanych jest 25 000 do 80 000 preparatów rocznie. Proponuje się, aby preparaty były sporządzane centralnie a ich interpretacja odbywała się w poszczególnych pracowniach
- Zaakceptowane przez FDA urządzenia do automatycznego skryningu są dostępne do skryningu tradycyjnych preparatów cytologicznych, zastosowanie ich w Wielkiej Brytanii znacząco obniży obciążenie pracowni oraz zmniejszy opóznienia.
Preparaty LBC i skryning HPV
- Wprowadzenie selekcji pacjentek w oparciu o wyniki testu HPV doprowadziło do obniżenia o 72% liczby powtórnych rozmazów cytologicznych, ale co najmniej podwoiło odsetek pacjentek kierowanych na badanie kolposkopowe
- W związku z tym, że obecnie nie ma przekonywujących dowodów na czułość testu HPV DNA, to pomimo obiecujących wyników finansowych należy zachować ostrożność w stosowaniu testu HPV jako kryterium selekcji.
Wnioski
- Dotychczasowe badania wskazują, że głównym powodem wprowadzenia metodyki LBC jest podniesienie wydajności programów skryningowych poprzez redukcję liczby rozmazów nie nadających się do oceny, wzrost wydajności pracowni i w przyszłości wprowadzenie zaumatyzowanego skryningu
- College ma zastrzeżenia co do danych dotyczących czułości metodyki i adekwatności rozmazów (które wpływają na wydajność)
- Trzeba wspomnieć, że metodyka LBC nie była przebadana w badaniach długoterminowych w krajach w których skryning cytologiczny wykonuje się co 3 do 5 lat.
- Ocena preparatów LBC nie jest zawyżona w aspekcie większej czułości w porównaniu z aktualnymi programami skryningowymi
- Szkolenie w zakresie interpretacji preparatów LBC musi być prawidłowo zorganizowane. Wymagane jest doświadczenie w interpretacji tradycyjnych rozmazów cytologicznych.